Klinik Araştırmalar Koordinasyon Birimi
BİRİM HAKKINDA
KURULUŞ GEREKÇEMİZ
Klinik araştırma sürecinin tüm paydaşları arasında yasal mevzuat ve uluslararası standartlar kapsamında koordinasyonu sağlamak amacıyla kurulmuştur.
MİSYONUMUZ
Dokuz Eylül Üniversitesinde yapılan klinik araştırma sayısı ve kalitesini artırmak, gönüllü güvenliğini geliştirmek, araştırmacı ve yardımcı klinik araştırma personelinin eğitimini desteklemek, klinik araştırmalarda organizasyon ve standardizasyonu sağlayarak insan ve toplum sağlığına katkıda bulunmaktır.
VİZYONUMUZ
Klinik araştırmaların gerektirdiği bürokratik süreçleri hızla çözümleyen, gönüllüler, destekleyiciler, araştırmacılar arasında etkin koordinasyon sağlayan, ulusal ve uluslararası mevzuat ve standartlara uyumlu yasal düzenlemelerle çalışan, kaliteli veri üreten, uygun gönüllü potansiyeli olan, altyapısı yeterli hastane ve deneyimli araştırmacılara sahip, ulusal ve uluslararası düzeyde tanınırlığı olan bir klinik araştırma merkezi olmaktır.
DEĞERLERİMİZ
- Paylaşımcılık
- Kazan kazan
- Ölçülebilirlik
- Şeffaflık
HEDEFLERİMİZ 1 – ÜNİVERSİTE İÇİN:
- Endüstri destekli araştırma fonlarından artan oranlarda pay almak
- Araştırmacının başlattığı klinik araştırmalar için ulusal ve uluslararası fon bulmak
- Kurumun klinik araştırma hizmetlerinde iyileştirme ve geliştirme faaliyetleri yürütmek
HEDEFLERİMİZ 2 – AKADEMİSYENLER İÇİN:
- Klinik çalışma disiplini kazanmak (Araştırmacı, araştırma hemşiresi, teknisyen, vb.)
- Genç akademisyenlerimize deneyim ve bilgi kazanma fırsatı sağlamak
- İlaç geliştirme süreci ve yeni tedavi alanları ile ilgili güncel eğitimler vermek
- Yüksek etki faktörlü dergilerde yayın sayısını artırmak
- Bilimsel ağ ve platformlara katılmak
- Ulusal ve uluslararası karar verici kurum ve kuruluşların komisyonlarında yer almak
HEDEFLERİMİZ 3 – GÖNÜLLÜLER İÇİN:
- Gönüllülere yenilikçi ilaçlara erken erişim imkânı sağlamak
- Karşılanmamış tedavi ihtiyaçlarına yönelik geliştirilen tedavilere tüm dünya ile eşzamanlı ulaşma fırsatı sunmak
- Yaşam süresi ve kalitesinin artırılmasına katkıda bulunmak
- Mevcut tedavilere alternatif olan tedavilere erişim imkânı sağlamak
- Nadir hastalıklardaki tedavi alternatiflerine erişim imkânı sağlamak
GERÇEKLEŞTİRDİKLERİMİZ
- Faz I Klinik Araştırma Merkezi faaliyet izin belgesi yenilenmiştir.
- Hastane altyapısında gerekli hazırlıkların planlaması tamamlanmıştır.
- Hastanenin klinik araştırmalara destek süreçleri gözden geçirilmiş, hedeflerimize odaklanacak düzeltme süreci belirlenmiştir.
- Kilnik araştırma merkezi bünyesinde ‘odaklanmış’ merkezi organizasyon yapısı oluşturulmuştur.
Klinik Araştırma Nedir?
Klinik araştırmalar, tıbbi veya biyolojik bilgilerimizin geliştirilmesi için insanlar üzerinde uygulanan sistematik biyomedikal araştırmalardır. İlaçlar ile yapılan klinik araştırmalar, ilgili ilaç adayının veya bilinen bir tedavi yönteminin farmakokinetik (vücudun ilaca etkisi), farmakodinamik (ilacın vücuda etkisi) ve tedavi (etkililik ve güvenlilik) verilerinin açıklığa kavuşturulması için yapılmaktadır. Bu sayede daha etkili ve güvenli tedavilerin topluma sunulması için gereken bilgiler elde edilmektedir.
Bir ülkenin sağlık araştırmaları alanında gelişebilmesi kaliteli klinik araştırma merkezleriyle mümkündür.
Klinik Araştırma Fazları
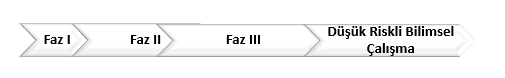
Ruhsat alma aşamasına kadar yapılması öngörülen ilaç klinik araştırmaları üç evreyi içerir. Her bir evre, bir öncekinden elde edilen bilgilerin doğrulanması ve olası eksikliklerin giderilmesi amacını taşır. Faz I, Faz II, Faz III olarak adlandırılan bu araştırma evrelerinden Faz I’ de hasta/sağlıklı gönüllüler, diğerlerinde ise hasta gönüllüler yer alır.
Ruhsat alınması ile klinik araştırmalara son verilmez. Pazarlama sonrası denetim adı verilen ruhsat evresinde de düşük riskli bilimsel çalışmalar yapılır. Bu evrede toplumda, çok sayıda insanda kullanılan ilaçların klinik çalışmalarda belirlenen etkililik ve güvenlilik özellikleri, daha çok gözlemsel çalışmalarla değerlendirilir. Ruhsat alımı sonrası yapılan bu çalışmalara farmakovijilans çalışmaları da denir.
Dört basamaktan oluşan bu araştırmaların amacı, önceden tasarlanmış ve belirlenmiş bir plan ve program çerçevesinde, alanında ve konusunda yetkin araştırıcılar tarafından seçilmiş hastalarda ve/veya sağlıklı gönüllülerde ilaç adayı ürünün, etkililiği ve güvenliliği ile ilgili her türlü bilginin, yetkin ve sorumlu araştırmacılar denetiminde en ince ayrıntısına kadar elde edilmesidir.
Böyle bir klinik denemeye başlayabilmek için öncelikle Etik Kurul onayı ve sonrasında Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu’nun olumlu görüşü, yani izninin alınması gerekir. Faz I, Faz II ve Faz III araştırma, ilaçların onay ve ruhsatının ön aşamalarıdır. Son yıllarda, özellikle hematoloji ve aonkoloji çalışmalarında Faz çalışmalarının içiçe geçtiği adaptif tasarımlı çalışmalar yapılmaktadır.
Başvuru süreci için tıklayınız.
PROJELERİMİZ için tıklayınız.

KADROMUZ
Birim Sorumlusu
Yeşim Tunçok
Birim Kalite Güvence Sorumlusu
Buket Erbayraktar
Birim İdari Sorumlu Personeli
Leyla Atılgan
Elifay Sert


